中国杭州和绍兴 2020年6月17日 -- 歌礼制药有限公司(香港联交所代码:1672)今日宣布,其合作伙伴Sagimet Biosciences(更名前为3-V Biosciences)今日公布非酒精性脂肪性肝炎(Non-alcoholic Steatohepatitis,简称NASH)候选药物TVB-2640(歌礼代号:ASC40)的二期临床(FASCINATE-1)数据,给药方式为口服、每日一次。初步数据显示,ASC40(TVB-2640)显著降低了肝脏脂肪含量(该试验的主要疗效终点),在50 mg剂量组中应答率为61%。另外,受试者还表现出肝功能和纤维化指标的改善。歌礼通过其子公司拥有在大中华区开发、制造和商业化ASC40(TVB-2640)及相关化合物的独家权益。 在签署独家开发协议的同期,Sagimet Biosciences完成由歌礼通过其子公司领投、新投资者和现有投资者跟投的E轮融资并募得2,500万美元。
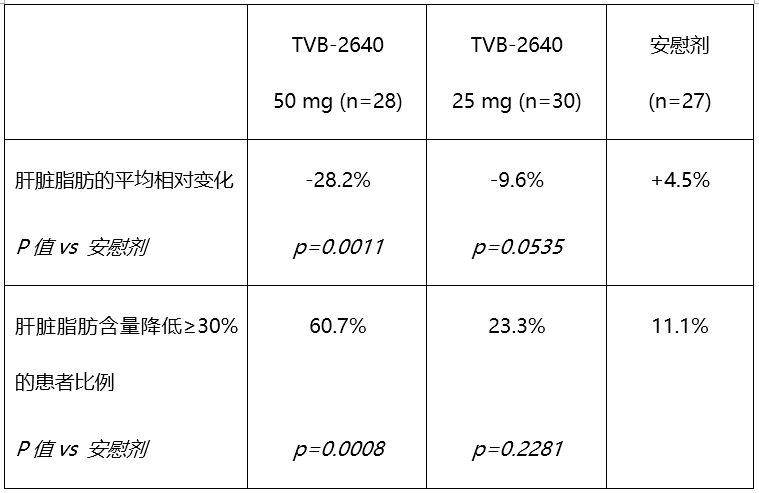
在这项随机、安慰剂对照的二期临床研究(FASCINATE-1)中,临床研究人员评估了TVB-2640在99名美国NASH患者中的安全性和有效性,每天给药一次,持续给药12周。入试者基线满足肝脏脂肪含量≥8%(由MRI-PDFF测定),且伴有肝纤维化F1-F3。该研究表明,在50 mg剂量组中,肝脏脂肪含量相对减少28.2%,而在安慰剂组中,肝脏脂肪含量相对增加4.5%。经过给药12周后,TVB-2640也显著降低了谷丙转氨酶(ALT)达20.4%, 降低低密度脂蛋白胆固醇(LDL-cholesterol)达7.6%。这些指标的下降表明肝功能和代谢水平得到改善。
TVB-2640表现出了良好的耐受性,良性不良事件主要为1级事件,无严重不良事件发生。
在中国开展的50 mg剂量临床试验的NASH患者筛选已经开始,拟入组25-30人。
歌礼还有另外两款内部开发的NASH候选药物。 ASC41是一款高活性、具选择性的甲状腺激素β受体(THR-beta)激动剂,其临床试验申请已获中国国家药品监督管理局批准。该项研究将以歌礼专有技术研发的口服片剂给药,预计将在2020年年底前获得一期临床研究的安全性、药代动力学和初步疗效(LDL-C)研究的顶线数据(topline results)。ASC42是针对另外一个靶点的处于pre-IND阶段的NASH候选药物。 歌礼在NASH领域布局的这3款候选药物处于不同开发阶段,可以单独使用或联合使用,使得歌礼具有国际竞争力。
关于歌礼
歌礼是一家拥有两个上市产品的创新研发驱动型生物科技公司,已在香港证券交易所上市(歌礼制药,1672.HK)。歌礼致力于开发抗病毒、脂肪性肝炎、肿瘤相关创新药,满足国内外患者需求。在具备深厚专业知识及优秀过往成就的管理团队带领下,歌礼已发展成为一体化平台型公司,涵盖了从新药发现和开发直到生产和商业化的完整价值链。歌礼的在研和已上市产品主要聚焦以下三大领域:1、慢性丙型肝炎(HCV):一个已上市产品(首个由中国本土企业开发的用于丙肝治疗的直接抗病毒药物戈诺卫®)、一个即将上市产品和两个在研产品。2、慢性乙型肝炎(HBV):一个已上市产品(与罗氏合作的用于乙肝、丙肝治疗的具有良好市场基础的长效干扰素派罗欣®)和三个在研产品。3、非酒精性脂肪性肝炎(NASH):三个在研产品。欲了解更多信息,请登录网站:www.ascletis.com。
详情垂询:
歌礼制药有限公司
李晨霖, +86-159-6815-8530
pr@ascletis.com
ir@ascletis.com